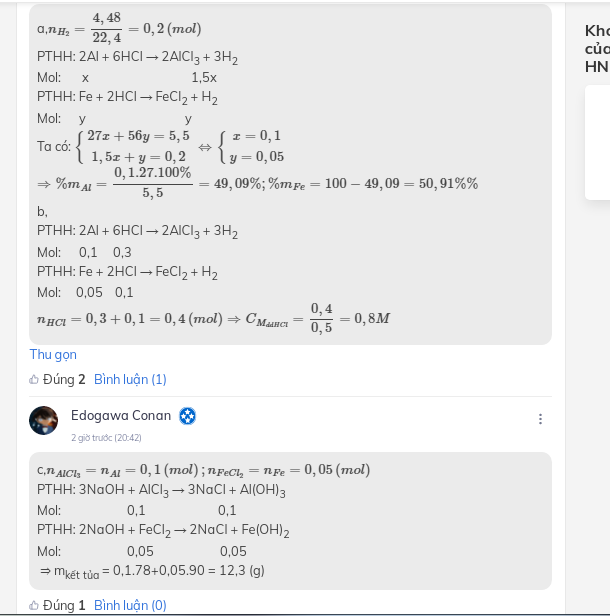
Bài 1 : Hòa tan 5,5g hôn hợp 2 kim loại Al và Fe trong 500ml dung dịch HCl thì thu được 4,48 lít khí H2 ở điều kiện tiêu chuẩn. Xác định thành phần % của môi kim loại trong hôn hợp ban đầu

Những câu hỏi liên quan
Hòa tan hoàn toàn 13,3 gam hôn hợp 2 kim loại Al và FeHòa tan hoàn toàn 13,3 gam hôn hợp 2 kim loại Al và Fe bằng dung dịch HCl dư thu được 7,84 lít H2 ở đktc.
Tính phần trăm khối lượng mỗi kim loại trong hỗn hợp ban đầu
Sửa đề : 13.9 (g)
\(n_{Al}=a\left(mol\right),n_{Fe}=b\left(mol\right)\)
\(\Rightarrow m=27a+56b=13.9\left(1\right)\)
\(n_{H_2}=\dfrac{7.84}{22.4}=0.35\left(mol\right)\)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
\(n_{H_2}=1.5a+b=0.35\left(2\right)\)
\(\left(1\right),\left(2\right):a=0.1,b=0.2\)
\(\%Al=\dfrac{0.1\cdot27}{13.9}\cdot100\%=19.42\%\)
\(\%Fe=100-19.42=80.58\%\)
Đúng 3
Bình luận (0)
Hòa tan 9g hóa học kim loại gồm Cu và Zn trong dung dịch HCL. Phản ứng xảy ra hoàn toàn thu được 896ml khí H2 ở điều kiện tiêu chuẩn, xác định thành phần phần trăm và khối lượng của kim loại trong hỗn hợp ban đầu.
PT: \(Zn+2HCl\rightarrow ZnCl_2+H_2\)
Ta có: \(n_{H_2}=\dfrac{0,896}{22,4}=0,04\left(mol\right)\)
Theo PT: \(n_{Zn}=n_{H_2}=0,04\left(mol\right)\Rightarrow m_{Zn}=0,04.65=2,6\left(g\right)\)
⇒ mCu = 9 - 2,6 = 6,4 (g)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Zn}=\dfrac{2,6}{9}.100\%\approx28,89\%\\\%m_{Cu}\approx71,11\%\end{matrix}\right.\)
Đúng 1
Bình luận (0)
hòa tan hoàn toàn 5,5g hỗn hợp 2 kim loại Al và Fe trong 500ml dung dịch HCL thì thu đc 4,958l khí h2 ở đk chuẩn ( 25 độ C , 1 bar)
Hòa tan 8 gam hỗn hợp Fe và Mg bằng dung dịch axit HCl thu được 4,48 lít khí hidro (điều kiện tiêu chuẩn). Tính khối lượng mỗi kim loại trong hỗn hợp ban đầu.
Đặt \(\begin{cases} n_{Fe}=x(mol)\\ n_{Mg}=y(mol) \end{cases}\Rightarrow 56x+24y=8(1)\)
\(n_{H_2}=\dfrac{4,48}{22,4}=0,2(mol)\\ PTHH:Fe+2HCl\to FeCl_2+H_2\\ Mg+2HCl\to MgCl_2+H_2\\ \Rightarrow x+y=0,2(2)\\ (1)(2)\Rightarrow \begin{cases} x=0,1(mol)\\ y=0,1(mol) \end{cases}\Rightarrow \begin{cases} m_{Fe}=0,1.56=5,6(g)\\ m_{Mg}=0,1.24=2,4(g) \end{cases} \)
Đúng 1
Bình luận (0)
hòa tan 8,4 g hỗn hợp gồm Fe và kim loại M vào dung dịch HCl dư thì thu được 4,48 lít khí h2 .nếu hòa tan 2,75 gam kim loại M thì không dùng hết 9,125 gam axit HCl.
1.xác định kim loại M
2.tính thành phần trăm về khối lượng của mỗi kim loại trong hỗn hợp ban đầu
Hòa tan 11 gam hỗn hợp Fe và Al bằng dung dịch axit h2so4 loãng dư thu được 8,96 lít khí hidro ( điều kiện tiêu chuẩn ). xác định thành phần phần trăm về khối lượng của mỗi kim loại
hòa tan hoàn toàn 5,5 g hỗn hợp 2 kim loại Al và Fe trong 500ml dd HCL thì thu đc 4,958 L khí h2 ở đk chuẩn ( 25 độ C , 1 bar)
a) xác định thàn phần phần trăm của mỗi kim loại trong hỗn hợp
b) Tính nồng độ mol của acid HCL
\(a)n_{H_2}=\dfrac{4,958}{24,79}=0,2\left(mol\right)\\ 2Al+6HCl\rightarrow2AlCl_3+3H_2\left(1\right)\\ Fe+2HCl\rightarrow FeCl_2+H_2\left(2\right)\\ n_{Al}=a;n_{Fe}=b\\ \left\{{}\begin{matrix}1,5a+b=0,2\\27a+56b=5,5\end{matrix}\right.\\ a=0,1\\ b=0,05\\ \%_{Al}=\dfrac{0,1.27}{5,5}\cdot100=49\%\\ \%_{Fe}=100-49=51\%\\ b)n_{HCl\left(1\right)_{ }}=0,1\cdot\dfrac{6}{2}=0,3\left(mol\right)\\ n_{HCl\left(2\right)}=0,05.2=0,1\left(mol\right)\\ n_{HCl}=0,3+0,1=0,4\left(mol\right)\\ C_{M_{HCl}}=\dfrac{0.4}{0,5}=0,8M\)
Đúng 2
Bình luận (0)
Hòa tan 5,5g hỗn hợp gồm Al và Fe cần 500ml dung dịch HCl thu được 4,48 lit khí (đktc)
a) xác định % khối lượng các kim loại trong hỗn hợp
b) TÍnh nồng độ mol của dung dịch HCl
c) khi cho dung dịch NaOH vào dung dịch muối, tính khối lượng kết tủa thu được lớn nhất
Hòa tan 10,8 gam hỗn hợp bột Fe và Cr trong dung dịch H2SO4 loãng thu được 4,48 lit khí H2 (điều kiện tiêu chuẩn). a. Xác định % khối lượng của mỗi kim loại trong hỗn hợp b. Tính khối lượng axít đã phản ứng
a) Gọi số mol Fe, Cr là a, b (mol)
=> 56a + 52b = 10,8 (1)
\(n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
PTHH: Fe + H2SO4 --> FeSO4 + H2
a---->a------------------->a
Cr + H2SO4 --> CrSO4 + H2
b--->b------------------->b
=> a + b = 0,2 (2)
(1)(2) => a = 0,1 (mol); b = 0,1 (mol)
=> \(\left\{{}\begin{matrix}\%Fe=\dfrac{0,1.56}{10,8}.100\%=51,85\%\\\%Cr=\dfrac{0,1.52}{10,8}.100\%=48,15\%\end{matrix}\right.\)
b) \(n_{H_2SO_4}=a+b=0,2\left(mol\right)\)
=> \(m_{H_2SO_4}=0,2.98=19,6\left(g\right)\)
Đúng 4
Bình luận (1)